


Метаболизм углеводов
Регуляция углеводного обмена
 А. Регуляция углеводного
обмена
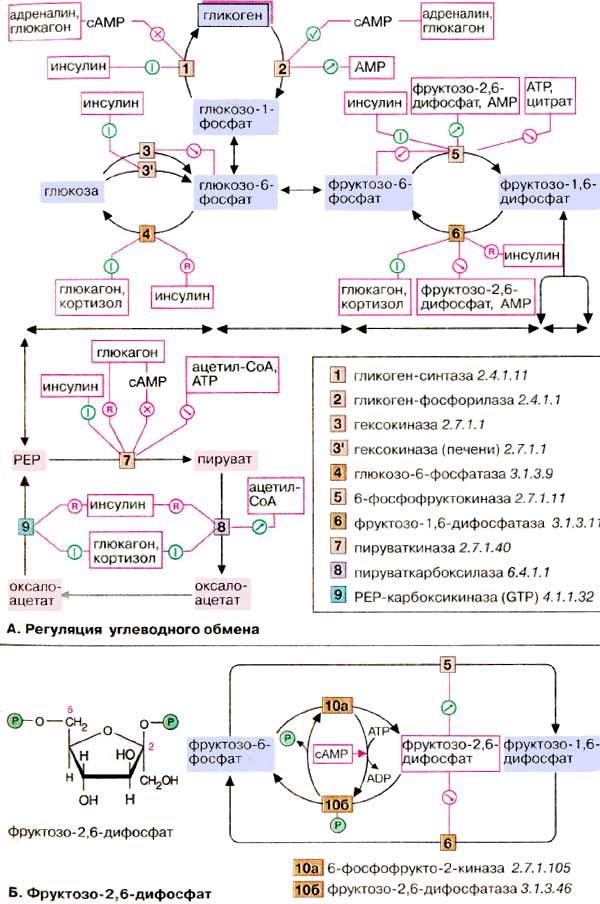
А. Регуляция углеводного
обмена
У высших организмов обмен углеводов
подвержен сложным механизмам регуляции, в которых участвуют гормоны,
метаболиты и коферменты. Представленная здесь схема относится к
печени, которая занимает в углеводном метаболизме центральное место (см.
с. 302). Некоторые из представленных механизмов не действуют в других
тканях.
Одной из важнейших функций клеток печени является накопление
избыточной глюкозы в виде гликогена и ее быстрое высвобождение по мере метаболической
необходимости (буферная функция). После полной мобилизации запасов гликогена
печень может поставлять глюкозу за счет синтеза de novo (глюконеогенез,
см. сс. 156, 232). Кроме того,
как и все ткани, она потребляет глюкозу путем гликолиза. Функции накопления
(синтеза) глюкозы в виде гликогена и его распада должны быть взаимосогласованы.
Таким образом, совершенно невозможно одновременное протекание гликолиза
и глюконеогенеза, как и синтеза и деградации гликогена. Согласование процессов
обеспечивается тем, что синтез (анаболизм) и распад (катаболизм) катализируются
двумя различными ферментами и контролируются независимо. На схеме показаны
только эти ключевые ферменты.
Гормоны. К гормонам, которые влияют на углеводный обмен,
принадлежат пептиды инсулин и глюкагон, глюкокортикоид кортизол
и катехоламин адреналин (см. сс. 362, 368).
Инсулин индуцирует (см.
с. 120) синтез de novo гликоген-синтазы [1],
а также некоторых ферментов гликолиза [3, 5, 7].
Одновременно инсулин подавляет синтез ключевых ферментов глюконеогенеза (репрессия,
[4, 6, 8, 9]). Глюкагон как антагонист инсулина
действует в противоположном направлении: индуцирует ферменты глюконеогенеза
[4, 6, 8, 9] и репрессирует пируваткиназу
[7], ключевой фермент гликолиза. Другие
аффекты глюкагона основаны на взаимопревращении ферментов и опосредованы
вторичным мессенджером цАМФ (сАМР, см. с. 114). По этому
механизму тормозится синтез гликогена [1] и активируется
расщепление гликогена [2]. Подобным образом действует
и адреналин. Торможение пируваткиназы [7]
глюкагоном также обусловлено взаимопревращением ферментов.
Глюкокортикоиды, прежде всего кортизол (см. с. 362),
индуцируют все ключевые ферменты глюконеогенеза [4, 6,
8, 9]. Одновременно они индуцируют ферменты деградации аминокислот и
обеспечивают тем самым глюконеогенез исходными соединениями.
Метаболиты. Высокие концентрации
АТФ (АТР) и цитрата тормозят гликолиз путем аллостерической
регуляции фосфофруктокиназы. Кроме того, АТФ тормозит
пируваткиназу. Ингибитором пируваткиназы является ацетил-КоА. Все эти
метаболиты образуются при распаде глюкозы (торможение конечным
продуктом). АМФ (AMP), сигнал дефицита АТФ, активирует расщепление
гликогена и тормозит глюконеогенез.
Б.
Фруктозо-2,6-дифосфат
Важную роль в обмене веществ в печени
играет фруктозо-2,6-дифосфат. Это сигнальное вещество образуется в
незначительных количествах из фруктозо-6-фосфата и выполняет чисто
регуляторную функцию: стимулирует гликолиз путем активации
фосфофруктокиназы и подавляет глюконеогенез с помощью торможения
фруктозо-1,5-дифосфатазы.
Образование и распад фруктозо-2,6-дифосфата катализируются
одним и тем же белком [10а и б]. В нефосфорилированной
форме этот белок вызывает образование фруктозо-2,6-дифосфата [10а].
После фосфорилирования цАМФ-зависимой киназой он действует как фосфатаза
[10б] и катализирует превращение фруктозо-2,6-дифосфата
в фруктозо-6-фосфат. В присутствии адреналина и глюкагона в клетках печени повышается
уровень цАМФ (см. с. 122), т.е. оба гормона воздействуют
как на гликолиз, так и на глюконеогенез. Суммарным результатом является быстрое
повышение уровня глюкозы в крови.