


Метаболизм. Ферменты
Активированные метаболиты
 Многие коферменты (см. сс. 108-111)
предназначены для активации менее реакционноспособных молекул или групп.
Активация заключается в образовании из соответствующей группы реакционноспособного
промежуточного соединения, которое может переноситься в экзоэргической реакции
на другую молекулу (см. с. 126). В качестве примера прежде
всего следует упомянуть кофермент А, который связывает и тем самым активирует
остатки жирных кислот благодаря образованию тиолсложноэфирной связи (см. сс.
58 и 110).
Многие коферменты (см. сс. 108-111)
предназначены для активации менее реакционноспособных молекул или групп.
Активация заключается в образовании из соответствующей группы реакционноспособного
промежуточного соединения, которое может переноситься в экзоэргической реакции
на другую молекулу (см. с. 126). В качестве примера прежде
всего следует упомянуть кофермент А, который связывает и тем самым активирует
остатки жирных кислот благодаря образованию тиолсложноэфирной связи (см. сс.
58 и 110).
АТФ и другие нуклеозидтрифосфатные
коферменты могут переносить не только фосфатные остатки, но и участвовать
также в реакциях активации. Здесь рассмотрены метаболиты или группы, которые
активируются при обмене веществ, связанном с нуклеозидами или нуклеотидами. В
дальнейшем такая активация будет продемонстрирована на примере метаболизма
сложных углеводов и липидов.
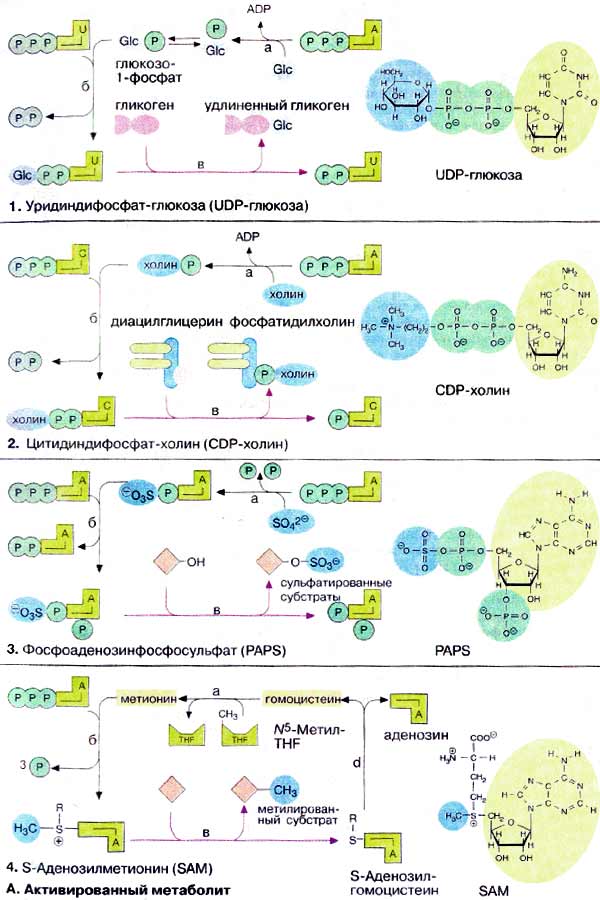
А. Активированный
метаболит
1. Уридиндифосфат-глюкоза
[УДФ-глюкоза (UDP-глюкоза)]
Встраивание остатков глюкозы в полимер, такой, как гликоген
или крахмал, является эндоэргическим процессом. Активация глюкозы происходит
в несколько стадий, при которых на один остаток глюкозы расходуются две молекулы
АТФ. После фосфорилирования свободной глюкозы с образованием глюкозо-6-фосфата
и изомеризации в глюкозо-1-фосфат (а) по реакции
с УТФ (UTP) (б) образуется УДФ-глюкоза, у которой
аномерная ОН-группа при атоме С1 углевода связана с фосфатом, Эта 'богатая энергией'
связь (ацеталь-фосфат) делает возможным экзоэргический перенос остатков глюкозы
на гликоген (в, см. сс. 122,
158) или другие акцепторы.
2. Цитидиндифосфат-холин
[ЦДФ-холин (CDP-холин)]
По аналогичному принципу активируется аминоспирт холин
для встраивания его в фосфолипид (см. с. 172). Холин прежде
всего фосфорилируется АТФ в холинфосфат (а), который
с отщеплением от ЦТФ дифосфата переходит в ЦДФ-холин. В отличие от схемы на
рис. 1, из ЦДФ-холина переносится не холин, а холинфосфат,
который образует с диацилглицерином фосфатидилхолин (лецитин).
3. Фосфоаденозинфосфосульфат [ФАФС
(PAPS)]
Сульфат-группы в различных биомолекулах проявляют себя как
сильные полярные группы, например, в глюкозаминогликанах (см. с. 336)
и конъюгатах стероидных гормонов с ксенобиотиками (см. с.
308). При синтезе 'активированного сульфата' (ФАФС) АТФ реагирует прежде
всего с неорганическим сульфатом с образованием аденозинфосфосульфата (АФС)
(а) - промежуточного соединения, содержащего уже
'богатый энергией' смешанный ангидрид фосфорной и серной кислот. На втором этапе
фосфорилируется 3'-ОН-группа АФС в АТФ-зависимой реакции. После переноса сульфатного
остатка на ОН-группу (в) побочным продуктом является аденозин-3',5'-дифосфат.
4. S-Аденозилметионин
(SAM)
В обмене веществ перенос C1-групп осуществляется
прежде всего коферментом тетрагидрофолатом [ТГФ (THF)], способным связывать
такие группы в различных стадиях окисления (см. срис. 111,
406). Кроме того, во многих реакциях метилирования
принимает участие "активированный метил" в форме S-аденозилметионина (SAM).
Так, SAM участвует в превращении норадреналина в адреналин (см. с. 342),
в инактивации норадреналина (путем метилирования фенольной ОН-группы) (см. с.
308), а также в образовании активной формы цитостатика
6-меркаптопурина (см. с. 388).
SAM образуется при разрушении белка из
аминокислоты метионина, на которую перекосится аденозильный остаток молекулы АТФ
(см. рис. 403). После переноса активированной метильной группы побочным продуктом
реакции является S-аденозилгомоцистеин, который может превращаться в две стадии
в метионин. При отщеплении остатка аденозина возникает небелковая
аминокислота гомоцистеин, на который с помощью
N5-метил-ТГФ снова переносится метильная группа (см. с. 106). Кроме
того, гомоцистеин может расходоваться также на образование пропионил-КоА (см. c.
403).