


Метаболизм. Энергетика
Цитратный цикл: реакции
 В
цитратном цикле (цикл лимонной кислоты; метаболический процесс, протекающий
в матриксе митохондрий) ацетильные остатки (CH3CO-) окисляются до
диоксида углерода (CO2). Полученные при этом восстановительные эквиваленты
переносятся на НАД+ или убихинон и включаются в дыхательную цепь
(см. с. 142). Центральная роль цитратного цикла в метаболизме
клетки рассматривается на с. 140.
В
цитратном цикле (цикл лимонной кислоты; метаболический процесс, протекающий
в матриксе митохондрий) ацетильные остатки (CH3CO-) окисляются до
диоксида углерода (CO2). Полученные при этом восстановительные эквиваленты
переносятся на НАД+ или убихинон и включаются в дыхательную цепь
(см. с. 142). Центральная роль цитратного цикла в метаболизме
клетки рассматривается на с. 140.
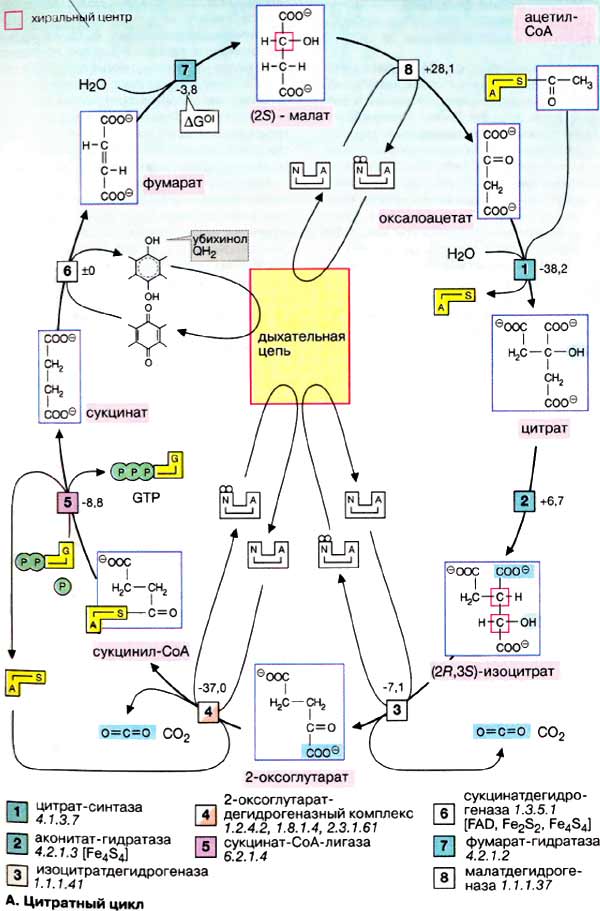
А. Цитратный цикл
Большая часть потребляемого в цитратном
цикле ацетил-КоА получает ацетильные остатки, образовавшиеся в результате
β-окисления жирных кислот (см. с. 166) и окислительного
декарбоксилирования пирувата, катализируемого пируватдегидрогеназой (см.
с. 136). Оба процесса протекают в матриксе митохондрий.
Окисление ацетильных остатков включает ряд промежуточных стадий,
образующих цикл: сначала ацетильная группа в реакции, катализируемой цитрат-синтазой
[1], конденсируется с молекулой оксалоацетата
с образованием цитрата (цикл получил свое название по продукту этой реакции).
На следующей стадии [2] цитрат изомеризуется
в изоцитрат с переносом гидроксильной группы внутри молекулы. При этом
промежуточный продукт реакции, ненасыщенный аконитат, остается во время реакции
связанным с ферментом (на схеме не показано). Поэтому фермент, катализирующий
реакцию, называют аконитат-гидратазой [2]
('аконитазой').
Свойства аконитат-гидратазы обеспечивают
абсолютную стереоспецифичность изомеризации. В то время как цитрат не
обладает хиральностью, изоцитрат содержит два асимметрических центра и может
существовать в четырех изомерных формах. Однако в цитратном цикле образуется
только один из стерео изомеров, (2R,3S)-изоцитрат (см. с. 16).
На следующей стадии изоцитратдегидрогеназа (3)
окисляет гидроксигруппу изоцитрата в оксогруппу с одновременным отщеплением
одной из карбоксильных групп в виде CO2 и образованием 2-оксоглутарата.
Последующее образование сукцинил-КоА [4],
включающее реакции окисления и декарбоксилирования, катализируется мультиферментным
комплексом, 2-оксоглутаратдегидрогеназой (дегидрогеназы кетокислот рассмотрены
на предыдущей странице). Расщепление тиолсложноэфирной связи сукцинил-КоА с
образованием сукцината и кофермента А, катализируемое сукцинат-КоА-лигазой
('тиокиназой' (5)], - высокоэкзоэргическая
реакция, энергия которой используется для синтеза фосфоангидридной связи ('субстратного
фосфорилирования', см. с. 126). В цитратном цикле
синтезируется не АТФ, как в большинстве таких реакций, а гуанозинтрифосфат
[ГТФ (GTP)], который легко превращается в АТФ нуклеозиддифосфаткиназой
(на схеме не показано).
В приведенных реакциях ацетильный остаток полностью окисляется
до CO2. Однако одновременно молекула переносчика оксалоацетата восстанавливается
в сукцинат. В трех последующих реакциях цикла сукцинат снова превращается в
оксалоацетат. Вначале сукцинатдегидрогеназа [6]
окисляет сукцинат в фумарат. В отличие от других ферментов цикла сукцинатдегидрогеназа
является интегральным белком внутренней митохондриальной мембраны. Поэтому ее
относят также к комплексу II дыхательной цепи. Сукцинатдегидрогеназа содержит
ФАД (FAD) в качестве простетической группы, однако фактическим акцептором электронов
является убихинон. Затем к двойной связи фумарата с помощью фумарат-гидратазы
('фумаразы', [7]) присоединяется вода и образуется
хиральный (2S)-малат. На последней стадии цикла малат окисляется
малатдегидрогеназой (8) в оксалоацетат
с образованием НАДН + Н+. Эта реакция замыкает цитратный цикл.
Общий баланс цитратного цикла
состоит в том, что из одного ацетильного остатка образуются 2 CO2, 3
НАДН + Н+ и одна молекула восстановленного убихинона
(QH2). При этом за счет восстановленных форм коферментов путем
окислительного фосфорилирования в клетке синтезируются 9, а с учетом
трансформации одной молекулы ГТФ - 10 молекул АТФ (см. с.
148).
Метаболизм. Энергетика